Pochopení kapacitního faktoru může redukovat problémy a vést k vývoji stabilnějších metod.
Při pohledu na data generovaná z HPLC analýzy je přirozené zaměřit se na retenční čas, asymetrii píků a účinnost. Tyto parametry umožní uživateli identifikovat a kvantifikovat analyty. Čím přesnější jsou tyto informace, tím větší je důvěra v identitu píku a koncentraci analytu.
Faktor kapacity je často přehlíženým parametrem separací, ale při správném použití může uživatele vést k vytvoření robustnější metodiky. Kapacitní faktor slouží k normalizaci retenční doby analytu na rozměry analytické kolony a je definován jako:
K’ = tr-t0/t0
Kde tr je retenční čas analytu a t0 je eluční čas nezadržené sloučeniny. Důležitost kapacitního faktoru lze nejlépe ilustrovat na příkladu:
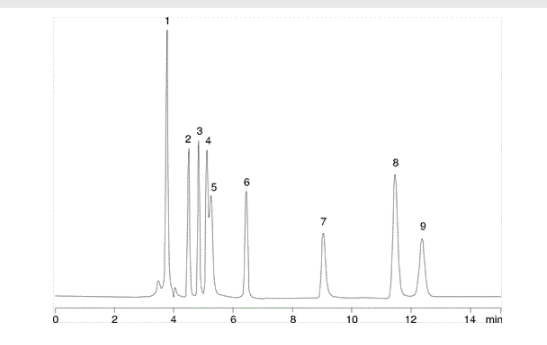
| 1. | Kyselina šťavelová |
| 2. | Kyselina vinná |
| 3. | Kyselina glykolová |
| 4. | Kyselina mravenčí |
| 5. | Kyselina pyrohroznová |
| 6. | Kyselina malonová |
| 7. | Kyselina octová |
| 8. | Kyselina maleinová |
| 9. | Kyselina citronová |
Zde máme separaci organických kyselin, probíhající na koloně C18, která je stabilní do 100% vodných podmínek. Mobilní fází je 20 mM pufr fosforečnanu draselného o pH 2,9 s průtokovou rychlostí 0,7 ml/min. Na první pohled je kyselina šťavelová zadržena téměř 4 minuty, ale při bližším pohledu je hodnota t0 pro tuto kolonu přibližně 3,7 minuty. Když to vezmeme v úvahu, je jasné, že kyselina šťavelová, velmi polární dikyselina, je v koloně sotva zadržena.
K’ = 3.9-3.7/3.7 = 0.054
To naznačuje, že kyselina šťavelová minimálně interaguje se stacionární fází během jejího průchodu kolonou. V takových případech bude retence analytů do značné míry ovlivněna malými, neúmyslnými změnami parametrů, včetně:
- Složení mobilní fáze
- pH mobilní fáze
- Síly ředícího roztoku vzorku
- Teploty
Taková metoda není robustní. Retence kyseliny šťavelové se bude lišit při každém cyklu, od kolony ke koloně a od jedné šarže mobilní fáze k druhé.
To vede k doporučení. Kdykoli se vyvíjejí metody, kapacitní faktory by se měly pohybovat v rozmezí 2–10. Viděli jsme potenciál problémů s kapacitními faktory menšími než 2, ale proč se zastavit na kapacitním faktoru 10?
Během izokratického běhu se šířka píku zvyšuje se zvyšujícím se retenčním časem v důsledku difúze. I když použití kolon s menšími částicemi a optimální průtoky pomohou tuto difúzi snížit, nelze ji vyloučit. Navíc vysoké kapacitní faktory nakonec vedou k dlouhým dobám běhu, které jsou v produktivním laboratorním prostředí obecně nežádoucí.
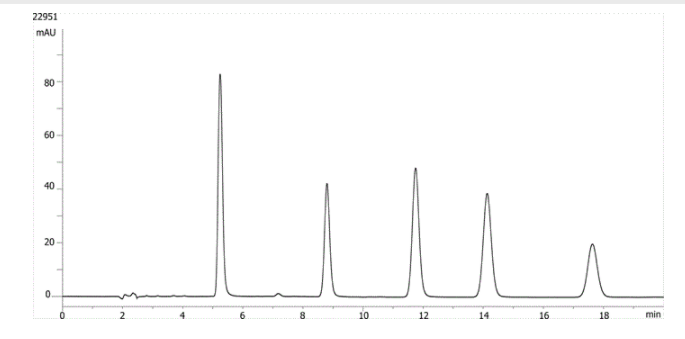
| 1. | Hydrokortison |
| 2. | Kortikosteron |
| 3. | 11-a-Hydroxyprogesteron |
| 4. | Kortizonacetát |
| 5. | 11-Ketoprogesteron |
Zde máme příklad steroidů na koloně 150 x 4,6 mm s průtokem 1 ml/min. 11-Ketoprogesteron se eluuje kolem 17,5 minuty s kapacitním faktorem přibližně 10,6. V tomto isokratickém běhu je patrné rozšíření píku, což naznačuje, že poslední eluční pík je na koloně zadržován příliš dlouhou dobu.
Porozumění obecným zásadám (kapacitní faktory mezi 2 a 10) je užitečné, ale zbývá nám otázka, jak je lze upravit?
Kapacitní faktor nepřímo souvisí s elutropickou silou mobilní fáze. Vyšší elutropní síla sníží kapacitní faktor a naopak. Pokud nízké faktory kapacity nelze zvýšit snížením elutropní síly mobilní fáze, může být nutné přejít na stacionární fázi, která může nabídnout větší retenci analytů například použitím polárnější stacionární fáze pro polární analyty.