Przegląd: Współcześni kandydaci na leki przedstawiają wiele wyzwań chromatograficznych; czy to wykrywanie, czy wydzielenie z koelucyjnego zanieczyszczenia, ale jedną z najczęstszych trudności jest zatrzymywanie i rozdzielanie związków polarnych, które nie są podatne na typowe warunki układu odwróconego faz C18.
Wiele tradycyjnych stacjonarnych faz RP nie zapewnia odpowiedniej retencji wielu z ciągle rosnącej liczby związków polarnych analizowanych za pomocą HPLC. Związki te są często albo niezatrzymywane w kolumnie, zatrzymują się tak słabo, że ich kształt pików jest niewiarygodny, lub są eluowane wspólnie z innymi słabo zatrzymywanymi substancjami. Wcześnie eluujące związki wychodzą także w strefie supresji jonów, co jest problematyczne dla osób używających aparatów LC-MS..
Ta wskazówka techniczna przedstawi HILIC jako alternatywne podejście, które jest szczególnie skuteczne w przypadku LC-MS. HILIC wykorzystuje duże ilości rozpuszczalnika organicznego do elucji związków polarnych, co pomaga poprawić ich efektywność jonizacji podczas analizy LC-MS.
Wskazówka: HILIC działa poprzez zatrzymywanie związków polarnych w wodnej warstwie, która powstaje na powierzchni cząsteczki krzemionki w wyniku polarnych oddziaływań z fazą stacjonarną (rys.1)
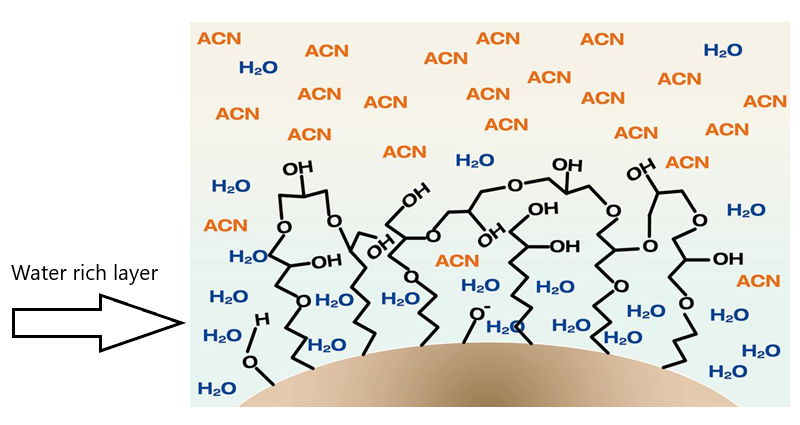
Acetonitryl (MeCN) jest słabym rozpuszczalnikiem w analizach HILIC, a bufor amonowy mocnym rozpuszczalnikiem. Sole amonu są krytyczne jako przeciwjon, ponieważ ułatwiają tworzenie podwójnej warstwy, niezbędnej dla rozdzielenia pokazanego na rys.1.
Mocno polarna faza stacjonarna przyciąga do swojej powierzchni warstwę wodną, co sprzyja zatrzymywaniu związków polarnych w fazie stacjonarnej. Związki polarne są wymywane, gdy zwiększa się ilość wody w fazie ruchomej, co zmniejsza zatrzymywanie polarnych analitów na polarnej fazie stacjonarnej, powodując elucję.
Ważne jest, aby przed użyciem w pełni zrównoważyć kolumnę HILIC, aby mieć pewność, że ta bogata w wodę warstwa miała odpowiedni czas na utworzenie się. Jeśli tak się nie stanie, nie zobaczysz ulepszenia w zatrzymywaniu swojego związku lub poprawy jakości Twojej metody.
Wspomnieliśmy o zastosowaniu buforów amonowych ale w metodzie HILIC jest kilka innych czynników, które są również krytyczne dla jej sukcesu.
Pierwszy to selektywność, dla której kluczowa jest właściwa kolumna. Podobnie jak w przypadku kolumn RP, istnieje wiele różnych faz stacjonarnych do chromatografii HILIC i każda z nich oferuje różne profile selektywności i korzyści. Zalecamy, aby zawsze starać się przetestować 3 fazy o różnej chemii, aby upewnić się, która zapewnia najlepszą selektywność dla danego zastosowania.
Rodzaje faz stacjonarnych HILIC, które możesz rozważyć, obejmują:
- Niezderywatyzowana krzemionka taka jak Kinetex HILIC
- Fazy diolowe jak: Luna HILIC
- fazy NH2
- Fazy jonowe/obojnacze
Jeśli chodzi o fazę ruchomą, ważne jest, aby używać acetonitrylu jako składnika organicznego - rozpuszczalniki protyczne, takie jak metanol, zakłócą ten dwuwarstwowy układ, o którym mówiliśmy. Ważna jest również ilość rozpuszczalnika organicznego. Zbyt wysoki procent składnika organicznego w początkowym punkcie gradientu skomplikuje i przedłuży równoważenie układu dwuwarstwowego; 90% organiki jest najlepsze do początkowych warunków metody.
Profil gradientowy powinien wynosić od 90% do 50% MeCN, jeśli to możliwe. Zapewnia to pełną równowagę układu dwuwarstwowego na początku gradientu. Jeśli do elucji związku wymagane są warunki z zawartością buforu wyższą niż 50%, wówczas prawdopodobnie metoda nie jest najlepiej dostosowana do HILIC i lepszym rozwiązaniem może być polarna faza stacjonarna typu C18. Po każdym przebiegu gradientu należy ponownie zrównoważyć kolumnę . Im wyższy procent buforu na końcu gradientu, tym dłużej będzie trwał proces ponownego równoważenia. Niecałkowite ponowne zrównoważenie kolumny doprowadzi do słabej odtwarzalności i niestabilności metody.
Ostatnim parametrem, który należy dokładnie rozważyć, jest pH. Należy przetestować co najmniej 2 różne pH; zwykle sugerujemy pH 3,2 przy użyciu mrówczanu amonu i 5,8 przy użyciu octanu amonu. Różne pH mogą prowadzić do znacząco różnych selektywności (rys. 2).
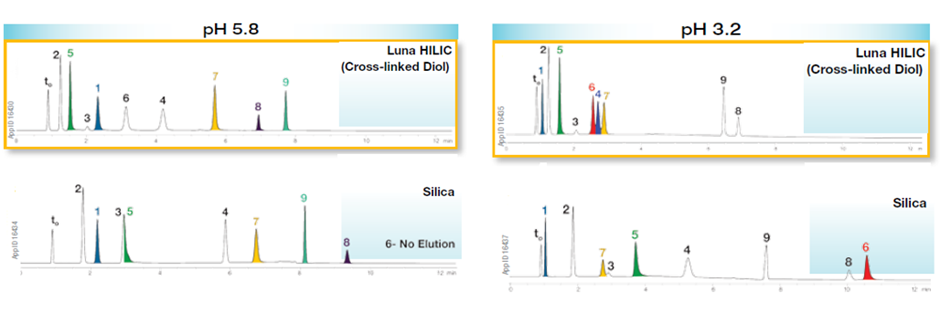
Duże zmiany kolejności elucji w zależności od chemii kolumny i warunków fazy ruchomej
Technika HILIC to niezwykle przydatne narzędzie poprawiające retencję związków polarnych. Technika ta może być sporym wyzwaniem przy poprawie jakości i stabilności metody, ale staranny dobór fazy ruchomej i parametrów metody mogą prowadzić do udanego rozdziału najtrudniejszych związków..
